Le syndrome de Kallmann-de Morsier: ą propos de trois cas
Halima Marhari, Fatima Zahra Chahdi Ouazzani, Hanan El Ouahabi, Laila Bouguenouch
Corresponding author: Halima Marhari, Service d'Endocrinologie, Diabétologie et Nutrition, CHU Hassan II, Fčs, Maroc 
Received: 16 Jan 2017 - Accepted: 29 Jun 2019 - Published: 18 Jul 2019
Domain: Endocrinology
Keywords: Hypogonadisme hypogonadotrope, mutation génétique, impubérisme, aménorrhée, anosmie
©Halima Marhari et al. Pan African Medical Journal (ISSN: 1937-8688). This is an Open Access article distributed under the terms of the Creative Commons Attribution International 4.0 License (https://creativecommons.org/licenses/by/4.0/), which permits unrestricted use, distribution, and reproduction in any medium, provided the original work is properly cited.
Cite this article: Halima Marhari et al. Le syndrome de Kallmann-de Morsier: ą propos de trois cas. Pan African Medical Journal. 2019;33:221. [doi: 10.11604/pamj.2019.33.221.11678]
Available online at: https://www.panafrican-med-journal.com//content/article/33/221/full
Le syndrome de Kallmann-de Morsier: ą propos de trois cas
Kallmann-de Morsier syndrome: about 3 cases
Halima Marhari1,&, Fatima Zahra Chahdi Ouazzani1, Hanan El Ouahabi1,2, Laila Bouguenouch2,3
1Service d'Endocrinologie, Diabétologie et Nutrition, CHU Hassan II, Fčs, Maroc, 2Faculté de Médecine et de Pharmacie de Fčs, Université Sidi Mohamed Ben Abdellah, Fčs, Maroc, 3Unité de Génétique Médicale et d'Oncogénétique, Laboratoire Centrale d'Analyses Médicales, CHU Hassan II, Fčs, Maroc
&Auteur correspondant
Halima Marhari, Service d'Endocrinologie, Diabétologie et Nutrition, CHU Hassan II, Fčs, Maroc
Le syndrome de Kallmann-de Morsier (KS) est une maladie génétique du développement du systčme olfactif caractérisée par l'association d'un hypogonadisme hypogonadotrophique par déficit en gonadolibérine (GnRH) et d'une anosmie ou hyposmie. Le diagnostic se fait le plus souvent ą l'adolescence devant une absence de puberté spontanée associée ą un trouble de l'odorat, avec visualisation sur l'IRM hypothalamo-hypophysaire d'une hypoplasie voire une aplasie des bulbes et/ou des lobes olfactifs. Parfois, le diagnostic peut źtre évoqué dans la petite enfance devant l'association d'une cryptorchidie et d'un micropénis. Une mutation dans l'un de ses gčnes connus n'est retrouvée que dans moins de 30% des cas et donc plusieurs autres gčnes restent ą découvrir. Grāce au traitement hormonal, la puberté se produit dans tous les cas, et la fertilité peut źtre obtenue dans la plupart des cas. Dans la présente étude, nous rapportons 3 cas de patients atteints de ce syndrome.
English abstract
Kallmann-de Morsier syndrome (KS) is a genetic disease of the olfactory system characterized by the association of hypogonadotropic hypogonadism also referred to as gonadotropin-releasing hormone (GnRH) deficiency and anosmia or hyposmia (with hypoplasia or aplasia of the olfactory bulbs). Apart from sporadic cases that occur most often, familial Kallmann’s syndrome is being described with increasing frequency. Diagnosis is mainly made in adolescents with absence of spontaneous puberty associated with smell disorders with hypoplasia or even aplasia of the bulbs and/or of the olfactory lobes on MRI. Sometimes, the diagnosis may be suspected in early childhood due to the association of cryptorchidism and micropénis. A mutation in one of known genes is only found in less than 30% of cases and, therefore, many other genes are still to be found. Hormone therapy allows pubertal growth in all cases and fertility can be obtained in most of the cases. We here report 3 cases of patients with this syndrome.
Key words: Hypogonadotrophic hypogonadism, genetic mutation, impuberism, amenorrhea, anosmia
Le syndrome de Kallmann-de Morsier (KS) ou dysplasie olfacto-génitale, est défini par l'association d'un hypogonadisme hypogonadotrope et d'une anosmie ou hyposmie [1] et se caractérise par une hétérogénéité ą la fois génétique et phénotypique. L'hypogonadisme est dū ą des anomalies du développement neuronal affectant la migration prénatale des neurones ą GnRH [2], alors que l'anosmie est secondaire ą une atrophie des bulbes et/ou des lobes olfactifs. Cette maladie touche environ 1 garēon sur 10000 et est 4 fois moins fréquente chez la fille, il est possible que cette prévalence féminine soit sous-estimée du fait d'un diagnostic féminin moins visible. Le diagnostic se fait le plus souvent ą l'adolescence devant une absence de puberté spontanée associée ą un trouble de l'odorat, avec visualisation sur l'IRM hypothalamo-hypophysaire d'une hypoplasie voire une aplasie des bulbes et/ou des lobes olfactifs. Sur le plan génétique, deux formes sont décrites : la forme familiale et la forme sporadique qui reste la plus fréquente [3]. A ce jour, huit gčnes ont été identifiés, néanmoins aucune mutation dans l'un de ses huit gčnes n'est retrouvée chez environ 60 ą 65% des patients. Sur le plan thérapeutique, le traitement hormonal a pour objectif de déclencher la puberté et de maintenir les caractčres sexuels secondaires. Par les trois cas cliniques, suivis en ambulatoire dans le service d'Endocrinologie du CHU Hassan II de Fčs, nous allons essayer de clarifier certains aspects clinico-biologiques, génétiques et radiologiques du KS chez une population marocaine.
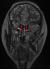
Cas 1: patient āgé de 20 ans, célibataire, sans antécédents pathologiques notables, qui présentait un impubérisme avec notion d'anosmie; chez qui l'examen clinique avait retrouvé un patient en surpoids, impubčre avec des testicules intra-scrotaux de 1,5 cm x 1,5 cm en bilatéral, un micropénis (-2,5DS), une pilosité pubienne stade I de Tanner, une pilosité axillaire absente et une gynécomastie stade III. Au bilan biologique un hypogonadisme hypogonadotrope était noté: FSH=0.07mUI/ml (0,95-11,95) LH=0.08mUI/ml (1,14-8,75), testostéronémie basse ą 0.5ng/ml, avec ą l'IRM hypothalamo-hypophysaire une agénésie des bulbes olfactifs (Figure 1). L'étude génétique n'avait pas objectivé de mutations au niveau des gčnes étudiés (KAL1, FGFR1, FGF8, CHD7, PROKR2, PROK2, HS6ST1, WDR11, SEMA3A, GNRH1, GNRHR, KISS1, KISS1R, SOX10, TAC3, TACR3), avec un caryotype 46 XY. Les autres axes hypothalamo-hypophysaires étaient indemnes et l'échographie rénale était sans particularité. Le patient était mis sous androgénothérapie (Enanthate de testostérone) avec une bonne évolution clinique: érection, éjaculation présentes, verge de 5cm. Pour sa gynécomastie le patient était adressé en chirurgie plastique pour une prise en charge esthétique.
Cas 2: patiente āgée de 22 ans, célibataire, sans antécédents pathologiques notables, qui présentait une aménorrhée primaire avec une anosmie chez qui l'examen clinique avait retrouvé une patiente maigre (IMC ą 16,8 kg/m2), impubčre: les seins stade II, la pilosité pubienne stade III de Tanner et la pilosité axillaire peu fournie. Sur le plan biologique, un hypogonadisme hypogonadotrope était objectivé: FSH =0,74mUI/ml (2-10), LH= 0,09mUI/ml (0,5-5), œstradiol < 10pg/ml et sur le plan radiologique, l'IRM hypothalamo-hypophysaire avait montré une hypoplasie des bulbes olfactifs et une hypotrophie des gouttičres olfactives. L'étude génétique était sans particularité notamment pas de mutations retrouvées avec un caryotype normal. L'exploration des autres axes hypothalamo-hypophysaires n'avait pas objectivé d'insuffisance et l'échographie rénale était normale. La patiente était mise sous traitement hormonale substitutif avec apparition des cycles menstruels réguliers.
Cas 3: patiente āgée de 30 ans, célibataire, sans antécédents pathologiques notables, qui présentait une aménorrhée secondaire sans anosmie ni hyposmie associée avec ą l'examen clinique: patiente en obésité totale avec des caractčres sexuels stade V de Tanner. Un hypogonadisme hypogonadotrope était noté: FSH=3,49mUI/ml (3-7), LH=1,55mUI/ml (0,5-5), œstradiol<10pg/ml (140-400), prolactine=21,58ng/ml, testosterone=0,41ng/ml, HGPO: glycémie ą T0=0,73g/l, ą T120=0,75g/l (hyper-insulinisme) et ą l'IRM hypothalamo-hypophysaire: une hypoplasie des bulbes olfactifs et hypotrophie des gouttičres olfactives. L'étude génétique n'avait pas objectivé de mutations, l'exploration des autres axes hypothalamo-hypophysaires étaient sans particularité et l'échographie rénale n'avait pas objectivé de malformations ni d'anomalies. La patiente était mise sous traitement hormonale substitutif avec apparition des cycles menstruels réguliers. Pour le syndrome métabolique: la patiente était mise sous mesures hygiéno-diététiques associées ą la metformine 1500mg/jr avec bonne évolution clinique et biologique.
Le syndrome de Kallmann a été décrit pour la premičre fois en 1944 par Franz Josef Kallmann, un généticien d'origine allemande émigré aux Etats-Unis; c'est une cause importante de défaut complet ou partiel, de développement pubertaire et résulte le plus souvent d'une sécrétion diminuée simultanée des 2 gonadotrophines hypophysaires, LH et FSH. Le tableau clinique du KS est variable suivant le sexe et l'importance du déficit. Il sera évoqué chez le garēon devant l'existence d'une cryptorchidie uni ou bilatérale et/ou d'un micropénis au cours de la période néonatale [4]. Le plus souvent, le diagnostic est suspecté devant une absence de développement pubertaire aprčs l'āge de 14 ans, ce qui est le cas chez le patient rapporté dans la premičre observation. Ą ce stade, la présence d'un micropénis et/ou d'une cryptorchidie est trčs en faveur de l'hypogonadisme hypogonadotrope congénital et rend improbable le diagnostic de retard pubertaire simple qui est une cause beaucoup plus fréquente de retard pubertaire avec gonadotrophines basses [5] cependant la détection prépubertaire est facilitée quand il existe déją un cas familial. Chez la fille, de mźme que notre deuxičme cas rapporté, le KS est révélé par une aménorrhée primaire dans plus de 90% des cas; le développement mammaire est trčs variable, souvent présent et parfois presque normal [6]; concernant la pilosité pubienne, elle peut źtre absente, clairsemée ou mźme normale. Sous une forme atténuée, l'hypogonadisme peut źtre limité ą une anovulation chronique, alors que la sécrétion d' œstradiol est adéquate pour le développement de l'endomčtre laissant apparaitre une seule menstruation (aménorrhée primo-ordinaire) ou une oligoménorrhée chronique ou un test au progestatif positif [7]. Dans tous les cas, il faudra rechercher des signes cliniques associés fortement évocateurs du syndrome de Kallmann comme une anosmie, des syncinésies (mouvements en miroir), anomalie de l'attention visuelle, anomalie de la motricité oculaire, ptosis, syndrome cérébelleux, surdité, pieds creux, palais creux, fente labiale et/ou palatine, agénésie dentaire agénésie rénale.
Devant une suspicion clinique d'un SK, un bilan sanguin s'impose, qui va révéler un hypogonadisme hypogonadotrope (testostéronémie <3,5nmol/l chez le garēon et des concentrations sériques d'œstradiol faibles chez la fille, parfois en dessous de la limite de détection), avec des taux plasmatiques de LH et FSH bas ou paradoxalement normaux. La GnRH a une courte demi-vie, et ne peut źtre mesurée dans le sérum; cependant chaque pulse de GnRH est synchrone avec un pulse de LH, cette derničre est donc la mesure inférée de la GnRH. Pour l'inhibine B, on la retrouve diminuée par rapport au stade pubertaire [8]. L'évaluation des fonctions antéhypophysaires est impérative afin d'évaluer l'ensemble des fonctions hypophysaires; cette précaution permet de ne pas méconnaītre d'autres insuffisances, tout particuličrement de l'axe corticotrope qui pourrait źtre peu parlante cliniquement. L'IRM s'est rapidement imposée comme examen de choix pour confirmer le diagnostic de syndrome de Kallmann de Morsier, en analysant les voies olfactives, situées au-dessus de la lame criblée de l'éthmoļde. Toutes les séquences permettent de déterminer l'absence ou non des bulbes olfactifs et l'épaisseur de la coupe ne doit pas excéder 3mm. Sa performance a été prouvée pour détecter de subtiles anomalies morphologiques notamment chez les enfants trop jeunes pour źtre testés du point de vue de l'olfaction [9] en montrant une agénésie ou une hypoplasie des bulbes olfactifs. Ainsi, il est impératif d'effectuer un examen uroradiologique détaillé chez les patients atteints de KS ą la recherche des anomalies rénales en raison de leur fréquence et leur diversité [10].
Le KS est génétiquement hétérogčnes et plusieurs modes de transmission génétique ont été décrits: récessif lié au chromosome X (KAL-1), autosomique dominant ou récessif; cependant, les cas sporadiques sont de loin les plus fréquents et seuls 30% environ des malades possčdent des mutations au niveau des gčnes connus (KAL1, KAL2, PROK2, PROKR2, FGF8, FGF17, IL17RD, DUSP6, SPRY4, FLRT3, SEMA3A, GNRHR, CHD7, SOX10 et IL17RD) [11]. Alors, nos patients rapportés font partie de la population des 60% sans mutation génétique décelée. Pour le diagnostic moléculaire, il est important notamment chez les malades désireux de procréer afin d'évaluer, avant l'induction hormonale de la fertilité, le risque encouru par la descendance. Le traitement de l'hypogonadisme en cas de KS vise aussi bien de déclencher le développement pubertaire avec des injections de testostérone chez les hommes et des oestro-progestatifs chez les femmes puis assurer le maintien des caractčres sexuels secondaires, que le développement de la fertilité, en faisant appel aux gonadotropines ou pulsatile GnRH pour obtenir la croissance testiculaire et la spermatogénčse chez les māles ou l'ovulation chez les femelles, ce qui permet de restaurer la fécondité dans une grande majorité des cas [12]. Pour le traitement hormonal transitoire post natal des garēons atteints pour simuler la poussée postnatale des gonadotrophines, son efficacité n'est pas encore démontrée au terme de son impact ultérieur sur leur vie [13]. Concernant le conseil génétique, il doit źtre adapté ą chaque famille et doit prendre en compte la forte variabilité phénotypique, y compris au sein d'une mźme famille.
Ą la lumičre de ce qui précčde, le KS est une pathologie rare dont le diagnostic est basé sur les preuves cliniques de la maturation sexuelle arrźtée ou incomplčte associées ą une anosmie ou hyposomie (qui est un critčre inconstant) et est confirmé par le dosage hormonal et l'IRM hypothalamo-hypophysaire centrée sur les bulbes olfactifs; toutefois l'étude génétique n'est pas toujours concluante vu que plusieurs gčnes restent ą découvrir, d'oł l'intérźt de mener dans l'avenir des études génétiques plus approfondies dans ce sens. Ainsi, grāce au traitement hormonal, la puberté se produit dans tous les cas; ą cet effet, un diagnostic précoce s'impose afin d'assurer une prise en charge optimale.
Les auteurs ne déclarent aucun conflit d'intérźts.
Tous les auteurs ont contribué ą la mise en œuvre et la réalisation de ce travail. Ils déclarent également avoir lu et approuvé la version finale du manuscrit.
Figure 1: IRM cérébrale montrant une agénésie bilatérale des bulbes olfactifs
- Nand N, Mittal R, Yadav M, Venu S, Deshmukh ARJ. Kallman Syndrome. Assoc Physicians India. 2016 Oct; 64(10): 106-107. PubMed | Google Scholar
- Catherine D, Luis T, Jean-pierre H. Kallmann de Morsier syndrome: genetics and pathophysiology. Médecine de la Reproduction, Gynécologie Endocrinologie. 2008; 2: 131-4. PubMed | Google Scholar
- Herauda MH.Management of an ovarian stimulation in case of a Kallmann-De Morsier syndrome. Gynecol Obstet Fertil. 2007 Jun; 35(6): 548-55. PubMed | Google Scholar
- Mitchell AL, Dwyer A, Pitteloud N, Quinton R. Genetic basis and variable phenotypic expression of Kallmann syndrome: towards a unifying theory. Trends Endocrinol Metab. 2011; 22(7): 249-58. PubMed | Google Scholar
- Kaplan JD, Bernstein JA, Kwan A, Hudgins L. Clues to an early diagnosis of Kallmann syndrome. Am J Med Genet. 2010; 152A(11): 2796-801. PubMed | Google Scholar
- Bry-Gauillard H. Congenital hypogonadotrophic hypogonadism in females: clinical spectrum, evaluation and genetics. Annales d'Endocrinologie. 2010 May; 71(3): 158-62. PubMed | Google Scholar
- Laroche E, Bricaire L, Christin-Maitre S. Diagnostic et prise en charge d'une aménorrhée chez l'adolescente.Archives de pédiatrie. 2013; 20(7): 817-822. PubMed | Google Scholar
- Klingmuller D, Dewes W, Krahe T, Brecht G, Schweikert HU. Related Magnetic resonance imaging of the brain in patients with anosmia and hypothalamic hypogonadism (Kallmann's syndrome). J Clin Endocrinol Metab. 1987; 65(3): 581-4. PubMed | Google Scholar
- Birnbacher R, Wandl-Vergesslich K, Frisch H. Diagnosis of X-recessive Kallmann syndrome in early infancy: evidence of hypoplastic rhinencephalon. Eur J Pediatr. 1994; 153(4): 245-7. PubMed | Google Scholar
- Miraoui H, Dwyer AA, Sykiotis GP, Plummer L, Chung W, Feng B et al. Mutations in FGF17, IL17RD, DUSP6, SPRY4, and FLRT3 are identified in individuals with congenital hypogonadotropic hypogonadism.Am J Hum Genet. 2013 May 2; 92(5): 725-43. PubMed | Google Scholar
- Jongmans MC, van Ravenswaaij-Arts CM, Pitteloud N, Ogata T, Sato N, Claahsen-van der Grinten HL et al. CHD7 mutations in patients initially diagnosed with Kallmann syndrome-the clinical overlap with CHARGE syndrome. Clin Genet. 2009 Jan;75(1): 65-71. PubMed | Google Scholar
- Grumbach MM. A window of opportunity: the diagnosis of gonadotropin deficienc. J Clin Endocrinol Metab. 2005 May; 90(5): 3122-7. PubMed | Google Scholar
- Cristina G, Jacques Y. Hypogonadismes hypogonadotrophiques congénitaux et syndrome de Kallmann chez l'homme. Presse Med. 2014; 43(2): 152-161. PubMed | Google Scholar