Mťtastase pleurale et pulmonaire díune polyadťnofibromatose dťgťnťrťť: ŗ propos díun cas
Kawtar El Hachimi, Hanane Benjelloun, Nahid Zaghba, Najiba Yassine
Corresponding author: El Hachimi Kawtar, Service des Maladies Respiratoires, CHU Ibn Rochd, Casablanca, Maroc 
Received: 14 Aug 2017 - Accepted: 12 Sep 2017 - Published: 06 Oct 2017
Domain: Oncology,Pulmonology,Gynecology
Keywords: Adénofibrome, adénofibromatose, pleurésie, métastase
©Kawtar El Hachimi et al. Pan African Medical Journal (ISSN: 1937-8688). This is an Open Access article distributed under the terms of the Creative Commons Attribution International 4.0 License (https://creativecommons.org/licenses/by/4.0/), which permits unrestricted use, distribution, and reproduction in any medium, provided the original work is properly cited.
Cite this article: Kawtar El Hachimi et al. Mťtastase pleurale et pulmonaire díune polyadťnofibromatose dťgťnťrťť: ŗ propos díun cas. Pan African Medical Journal. 2017;28:115. [doi: 10.11604/pamj.2017.28.115.13599]
Available online at: https://www.panafrican-med-journal.com//content/article/28/115/full
Original article 
Mťtastase pleurale et pulmonaire díune polyadťnofibromatose dťgťnťrťť: ŗ propos díun cas
Mťtastase pleurale et pulmonaire díune polyadťnofibromatose dťgťnťrťť: à propos díun cas
Pleural and lung metastasis from degenerated multiple adenofibromas: about a case
Kawtar El Hachimi1,&, Hanane Benjelloun1, Nahid Zaghba1, Najiba Yassine1
1Service des Maladies Respiratoires, CHU Ibn Rochd, Casablanca, Maroc
&Auteur correspondant
El Hachimi Kawtar, Service des Maladies Respiratoires, CHU Ibn Rochd, Casablanca, Maroc
La polyadťnofibromatose ou líadťnofibromatose est dťfinie par la prťsence díau moins 3 adťnofibromes, uni ou bilatťraux atteignant une taille importante responsable de troubles trophiques. Nous rapportons une observation colligťe au service des maladies respiratoires du Centre Hospitalier Universitaire Ibn Rochd de Casablanca. Il síagit díune patiente ‚gťe de 46ans, suivie depuis lí‚ge de 30 ans pour une adťnofibromatose bilatťrale opťrťe ŗ 4 reprises. Suite ŗ un bilan prťopťratoire díune mastectomie bilatťrale, une radio du thorax a ťtť rťalisťe objectivant un hťmithorax droit opaque avec refoulement des ťlťments du mťdiastin. Líexamen clinique retrouvait un syndrome díťpanchement liquidien de líhťmithorax droit et une adťnopathie cervicale sus claviculaire gauche. La ponction biopsie pleurale confirmait la localisation pleurale díun carcinome peu diffťrenciť et invasif compatible avec une origine mammaire. La bronchoscopie aprŤs ťvacuation pleurale objectivait un aspect infiltrť de tout líarbre bronchique, dont les biopsies concluaient au mÍme rťsultat anatomopathologique. Le traitement prťconisť ťtait une polychimiothťrapie. Líťvolution ťtait marquťe par líapparition de mťtastases hťpatiques. A travers cette observation, nous concluons que les adťnofibromes nťcessitent une surveillance rťguliŤre vu le risque de dťgťnťrescence vers le cancer du sein qui est une cause frťquente de mťtastases pleuropulmonaires.
English abstract
Multiple adenofibromas or adenofibromatosis is characterized by the presence of at least 3 mono- or bilateral adenofibromas increasing significantly in size, causing trophic disorders. We report the case of a 46-year old female patient who had been followed up since she was 30 years old for bilateral adenofibromatosis that required 4 surgical procedures. Patientís medical data were collected in the Department of Respiratory Diseases at the Ibn Rochd University Hospital Center, Casablanca. Basing on preoperative assessment before bilateral mastectomy, the patient underwent chest X-ray that showed opaque right hemithorax exerting compression on the mediastinum. Clinical examination showed effusion syndrome in the right hemithorax and left supraclavicular cervical adenopathy. Pleural puncture biopsy confirmed the presence of poorly differentiated invasive carcinoma in the pleura, supporting breast origin. Bronchoscopy after pleural puncture objectified infiltration of the whole bronchial tree; biopsies confirmed the anatomopathological results. The recommended treatment strategy was based on multidrug chemotherapy. Patientís evolution was marked by the occurrence of hepatic metastases. This study shows that adenofibromas require regular monitoring given the risk of trasformation to breast cancer, which is a frequent cause of pleuropulmonary metastases.
Key words: Adenofibroma, adenofibromatosis, pleurisy, metastasis
Les fibroadťnomes ou adťnofibromes (AF) sont des lťsions bťnignes le plus souvent rencontrťes chez líadolescente et la jeune femme de la deuxiŤme et la troisiŤme dťcennie [1]. Líadťnofibrome est líune des principales lťsions ťpithťliales bťnignes sans risque carcinologique. Ce dernier pourrait correspondre au risque de dťgťnťrescence rťvťlant une lťsion maligne [2]. Leur taille est gťnťralement infťrieure ŗ 3 centimŤtres [2]. Adénofibromatose ou maladie poly-adénofibromatose est dťfinie par des adťnofibromes multiples qui síobservent dans 10 ŗ 20% des cas, de faÁon synchrone ou successive, particuliŤrement chez les jeunes filles de race noire [3]. Les métastases pleuro-pulmonaires des cancers du sein sont fréquentes. Elles viennent en 3Ťme position aprŤs les mťtastases ganglionnaires et hťpatiques et ils sont retrouvťs dans 30% des autopsies de patients porteurs dīune nťoplasie [4].
Il síagit díune femme ‚gťe 46 ans, troisiŤme pare, suivie pour adťnofibromatose bilatťrale ou polyadťnofibromatose depuis lí‚ge de 30 ans, opťrťe ŗ quatre reprises pour des adťnofibromes gťants en raison díune gÍne esthťtique et fonctionnelle. La patiente est adressťe en consultation de pneumologie pour un ťpanchement pleural liquidien droit dťcouvert fortuitement lors díun bilan prť-opťratoire pour une ťventuelle mastectomie bilatťrale.
†
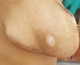
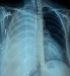
Líexamen du thorax rťvťlait un syndrome díťpanchement liquidien droit. Líexamen mammaire rťvťlait des seins trŤs augmentťs de volume, asymťtriques, siŤges de masses de tailles diffťrentes, non douleureuses, sans signes inflammatoires en regard, ainsi que trois cicatrices propres de chirurgie des adťnofibromes (Figure 1, Figure 2). Le reste de líexamen somatique trouvait une adťnopathie sus claviculaire gauche infracentimťtrique, sans signes inflammatoires en regard, reconnue par la patiente depuis un mois. La mammographie a montrť aussi des multiples masses de tailles diffťrentes (Figure 3). A la radiographie du thorax, on a notť un hťmithorax droit opaque avec refoulement des ťlťments du mťdiastin (Figure 4). Le complťment díimagerie (TDM thoracique) objectivait une pleurťsie droite de grande abondance. A la ponction pleurale, la plŤvre ťtait fine et le liquide ťtait sťrohťmatique. La ponction biopsie pleurale ťtait en faveur díune localisation pleurale díun carcinome peu diffťrenciť et invasif compatible avec une origine mammaire. Les ponctions pleurales ťvacuatrices ont totalisť deux litres de liquide sťrohťmatique. Une bronchoscopie faite aprŤs ťvacuation pleurale a montrť une infiltration tumorale de tout líarbre bronchique droit rťduisant le calibre de tous les orifices devenus incathťtťrisables.†
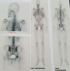
Les rťsultats des biopsies bronchiques concordaient avec ceux de la ponction biopsie pleurale. Il síagit díun carcinome peu diffťrenciť et invasif compatible avec une origine mammaire, dont líťtude immunohistochimique a montrť líabsence de surexpression de líHER2 par les cellules tumorales (HER2 score 0). Dans le cadre du bilan díextension, la tomodensitomťtrie (TDM) cťrťbrale est revenue normale ainsi que la TDM abdomino-pelvienne. Par contre, la scintigraphie osseuse a rťvťlť un foyer díhyperfixation modťrťe de C2, un foyer díhyperfixation assez intense de D9, un foyer díhyperfixation du bord droit du corps sternal, et un foyer díhyperfixation intense de la tÍte humťrale droite (Figure 5). Ces foyers ťtaient en faveur de localisations osseuses secondaires. La dťcision de la rťunion de concertation pluridisciplinaire a ťtť une polychimiothťrapie ŗ base de taxanes. Cliniquement aprŤs trois cures de chimiothťrapies, on a notť une rťgression des masses mammaires et persistance des adťnopathies. La TDM thoraco abdomino-pelvienne de contrŰle a montrť des infiltrats pulmonaires droits, et une hťpatomťgalie siŤge de 8 nodules de taille diffťrente, en faveur de lťsions secondaires.
Les adťnofibromes (AF) ou fibroadťnomes du sein sont des tumeurs bťnignes ŗ prolifťration intraparenchymateuse ŗ partir des canaux intra-lobulaires et des acinis. Les adťnofibromes multiples sont appelťs adťnofibromatose ou poly-adťnofibromatose. Lorsque la taille est supťrieure ŗ 5 centimŤtres avec une croissance rapide, on parle díadťnofibrome gťant [5]. Líadťnofibrome est soit de type ę classique Ľ sur le plan histologique, dťfini alors par sa taille ou par son poids dťpassant 500g, soit de type juvťnile síil possŤde un stroma particuliŤrement cellulaire, caractťristique ŗ cet ‚ge [6,7]. Il níexiste pas de donnťes díincidence des adťnofibromes dans la population gťnťrale. Les AF reprťsentent environ 50% de toutes les biopsies du sein. Ce taux arrive ŗ 75% pour les biopsies chez les femmes de moins de 20 ans [8,9].
†
Dans la poly-adťnofibromatose, les masses mammaires peuvent entrainer une gÍne esthťtique et fonctionnelle comme nous líavons constatť dans notre observation. Les mťcanismes ŗ la base de la genŤse et de la croissance des fibroadťnomes sont peu connus [2,10]. En pratique, il peut Ítre difficile devant la multiplicitť des nodules, de les comptabiliser [3]. Le risque relatif de dťvelopper un cancer pour une jeune femme porteuse de fibroadťnome sans antťcťdent familial níest pas augmentť [2]. La transformation maligne de la composante ťpithťliale des lťsions díadťnofibromes est considťrťe comme rare. Líincidence rapportťe varie de 0,002% ŗ 0,0125% [8]. Certains auteurs rapportent une coexistence de líadťnofibrome avec des carcinomes lobulaires in situ, des carcinomes lobulaires infiltrants, des carcinomes canalaires in situ et des carcinomes canalaires invasifs. Líincidence de cette coexistence varie de 2/1000 ŗ 1,25/1000 dans les adťnofibromes prouvťs histologiquement [11,12]. En cas de diagnostic díadťnofibrome ŗ la biopsie percutanťe, avec une discordance radioclinique, ou associant des lťsions complexes ou prolifťratives ou un antťcťdent familial de cancer, il semble lťgitime de discuter la prise en charge en rťunion de concertation multidisciplinaire et une surveillance est nťcessaire afin díťviter les interventions itťratives. Les modalitťs de prise en charge thťrapeutique sont un traitement díexťrŤse ou destructeur, un traitement par exťrŤse percutanťe guidťe par imagerie ou un traitement mťdical ŗ base du TamoxifŤne, ŗ la posologie de 20mg/jour [4,13]. Quand líaugmentation de la taille est rapide, le National Cancer Institute recommande une biopsie interventionnelle ou une exťrŤse chirurgicale [14]. Si líexťrŤse chirurgicale est dťcidťe pour un adťnofibrome, les incisions directes peuvent Ítre privilťgiťes afin díobtenir un meilleur rťsultat esthťtique. Líabord axillaire est associť ŗ un rťsultat esthťtique satisfaisant et une grande satisfaction des patientes selon une ťtude rťtrospective portant sur 50 patientes [15]. Líabord sous mammaire est associť ŗ la persistance díune asymťtrie mammaire post opťratoire [7], comme nous líavons constatť dans notre observation.†
En cas díun nodule gÍnant de 4 ŗ 5 centimŤtres, ou plus une exťrŤse chirurgicale sera pratiquťe, dans la crainte díune tumeur phyllode du sein (TPS) qui est une tumeur mammaire rare associant une double composante lťsionnelle fibro-ťpithťliale. Ces lťsions reprťsentent moins de 0,5% de líensemble des tumeurs du sein et seulement 2,5% des tumeurs fibro-ťpithťliales. Selon líorganisation mondiale de la santť (OMS) proposťe en 1981, il est usuel de distinguer trois catťgories de TPS: grade 1 (bťnin), grade 2 (borderline), grade 3 (malin) [16]. A líinverse, on peut observer une diminution de la taille significativement plus frťquente chez les jeunes filles de moins de 20 ans, que líadťnofibrome soit unique ou multiple, infťrieur ou supťrieur ŗ 2 cm [3].†
Les mťtastases pleuro-pulmonaires (MPP) ont une prťvalence de 30 ŗ 50% chez les patients porteurs de nťoplasie thoracique ou extrathoracique [17]. Chez environ 10% des patients qui prťsentent un ťpanchement pleural malin, le site primitif nīest pas retrouvť [18]. Le carcinome mammaire est la seconde cause dīťpanchement malin (25%) aprŤs le cancer du poumon. Les mťtastases pulmonaires des cancers du sein sont frťquemment retrouvťes dans la littťrature et surviennent essentiellement par voie hťmatogŤne ou lymphatique, elles reprťsentent 20 ŗ 35% des sťries [19]. Le dťveloppement du foyer pleural initial pourrait sīeffectuer ŗ partir dīune extension tumorale directe par contiguÔtť ou ťgalement dīune extension via les lymphatiques ou les vaisseaux sanguins. Aussi, des mťtastases hťpatiques et osseuses peuvent survenir de faÁon simultanťe au cours de nťoplasies du sein [4] et que cíest les cancers du sein sans rťcepteur hormonal qui fabriquent des mťtastases hťpatiques (le cas de notre observation), pulmonaires, cťrťbrales et mťningťes.
Suite ŗ notre observation, nous concluons que líadťnofibromatose nťcessite une surveillance ťtroite dans la crainte díune dťgťnťrescence maligne menant ŗ un cancer du sein responsable de mťtastases frťquentes.
Les auteurs ne dťclarent aucun conflit d'interÍts.
Tous les auteurs ont lu et approuvť la version finale du manuscrit.
Figure 1: image montrant des seins asymťtriques (vue de face)
Figure 2: image montrant des seins asymťtriques (vue de profil)
Figure 3: mammographie montrant de multiples masses au niveau du sein
Figure 4: radio du thorax face montrant un hťmithorax droit opaque avec refoulement des ťlťments du mťdiastin
Figure 5: scintigraphie osseuse qui montre des foyers de localisations osseuses secondaires
- Carter BA, Page DL, Schuyler P, Parl FF, Simpson JF, Jensen RA et al. No elevation in long-term breast carcinoma risk for women with fibroadenomas that contain atypical hyperplasia. Cancer. 2001;92(1):30-6. PubMed | Google Scholar
- Croce S, Bretz-Grenier MF, Mathelin C. Les principales lťsions mammaires epitheliales benignes et ŗ risque - Prise en charge diagnostique et thťrapeutique. Gynecol Obstet Fertil. 2008;36(7-8):788-799. Google Scholar
- Boisserie-Lacroix M, Lippa N, Ferron N, Hurtevent-Labrot G, Bullier B. Pathologie mammaire de líadolescente et de la jeune Fille. J femme. 2013;23(2):70-75. Google Scholar
- Badri F, Ait Batahar S, El Idrissi S, Sajiai H, Serhane H, Amro L. Mťtastases pleuro-pulmonaires des nťoplasies extra-thoraciques. Pan Afr Med J. 2017;26:44. Google Scholar
- Dolmans GH, Hoonergen NM, van Rappard JH. Giant fibroade-noma of one breast: immediate bilateral reconstruction. J PlastReconstr Aesthet Surg. 2007;60(10):1156-7. PubMed | Google Scholar
- Boisserie-Lacroix M, Ferron S, Lippa N, Ziadť C, Hurtevent-Labrot G. Surveillance des lťsions solides multiples. Imager de la Fem. 2016;26(2):109-115. Google Scholar
- Boisserie-Lacroix M, Bokobsa J, Boutet G, Colle M, Hockť C, Le Treut A. Sťnologie de líenfant et de líadolescente. Mťdecine Sciences. 1998:183. Google Scholar
- Bendifallaha S, Canlorbe G. Prise en charge des tumeurs bťnignes du sein ťpidťmiologiquement frťquentes de type adťnofibrome, phyllode (grade 1 et 2) et papillome: recommandations. Journal J Gynecol Obstet Biol Reprod. 2015;44(10):1017-1029. Google Scholar
- Schuerch C, Rosen PP, Hirota T, Itabashi M, Yamamoto H, Kinne DW et al. A pathologic study of benign breast diseases in Tokyoand New York. Cancer. 1982;50(9):1899-903. PubMed | Google Scholar
- Sapino A, Bosco M, Cassoni P, Castellano I, Arisio R, Cserni G et al. Estrogen receptor-beta is expressed in stromal cells of fibroadenoma and phyllodes tumors of the breast. Mod Pathol. 2006;19(4):599Ė606. PubMed | Google Scholar
- DeschÍnes L, Jacob S, Fabia J, Christen A. Beware of breast fibroadenomas in middle-aged women. Can J Surg. 1985;28(4):372-4. PubMed | Google Scholar
- Pick PW, Iossifides IA. Occurrence of breast carcinoma withina fibroadenoma: a review. Arch Pathol Lab Med. 1984;108(7):590-4. Google Scholar
- Viviani RSDO, Gebrim LH, Baracat EC, De Lima GR. Evaluation of the ultrasonographic volume of breast fibroa-denomas in women treated with tamoxifen. Minerva Ginecol. 2002;54(6):531-5. PubMed | Google Scholar
- Parickh JR. ACR appropriateness criteria on palpable breast masses. J Am Coll Radiol. 2007;4(5):2858. Google Scholar
- Khan PS, Hayat H, Hayat G. Transaxillary approach withuse of traction suture for excision of breast fibroade-noma: a new technique and its results. Surg Innov. 2012;19(1):NP10-3. PubMed | Google Scholar
- Bocker W. WHO classification of breast tumors and tumors of the female genital organs: pathology and genetics. Verh Dtsch Ges Pathol. 2002;86:116-9. PubMed | Google Scholar
- Johnson RM, Lindskog GE. 100 cases of tumor metastatic to lung and mediastinum: treatment and results. JAMA. 1967;202(2):94-98. PubMed | Google Scholar
- Sahn SA. State of the art: the pleura. Am Rev Respir Dis. 1988;138(1):184-234. PubMed | Google Scholar
- Ettensohn DB, Bennett JM, Hyde RW. Endobronchial metastases from carcinoma of the breast. Med Pediatr Oncol. 1985;13(1):9-13. PubMed | Google Scholar